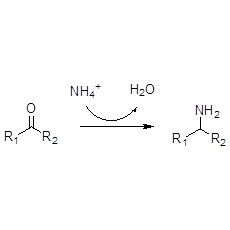
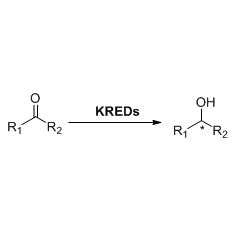
Reduktaza ene (ERED)
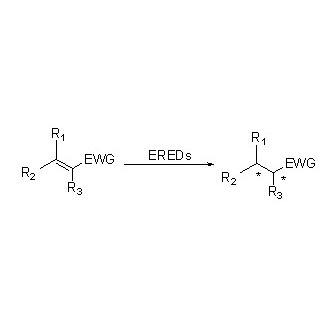
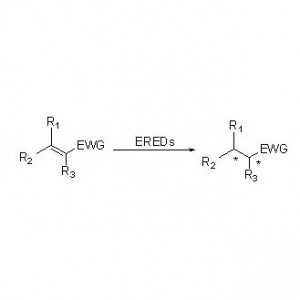
ES-ERED katalizują różne typy substratów ze względu na ich szerokie spektrum. Ogólnie rzecz biorąc, C=C związków α, β-nienasyconych z grupami absorbującymi elektrony (w tym ketonów, aldehydów, grup nitrowych, kwasów karboksylowych, estrów, bezwodników, laktonów, imin itp.) są łatwo redukowane przez ES-ERED, ale nieaktywowane wiązania podwójne nie ulegają redukcji.
Istnieje 46 rodzajów produktów enzymatycznych ERED (numeracja od ES-ERED-101 do ES-ERED-146) opracowanych przez firmę SyncoZymes.
Mechanizm katalityczny:
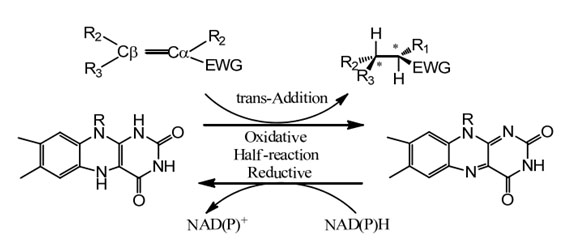
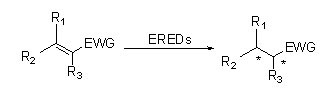
| Enzymy | Kod produktu | Specyfikacja |
| Proszek enzymatyczny | ES-ERED-101~ ES-ERED-146 | zestaw 46 reduktaz enezyny, po 50 mg każda, 46 sztuk * 50 mg / sztuka, lub inna ilość |
| Zestaw do badań przesiewowych (SynKit) | ES-ERED-4600 | zestaw 46 reduktaz enezyny, po 50 mg każda, 46 sztuk * 50 mg / sztuka, lub inna ilość |
★ Wysoka specyficzność substratowa.
★ Silna selektywność chiralna.
★ Wysoka konwersja.
★ Mniej produktów ubocznych.
★ Łagodne warunki reakcji.
★ Przyjazne dla środowiska.
★ Wysoki poziom bezpieczeństwa.
➢ Zwykle układ reakcji powinien obejmować substrat, roztwór buforowy (optymalne pH reakcji), koenzymy (NAD(H) lub NADP(H)), układ regeneracji koenzymów (np. glukozę i dehydrogenazę glukozową) oraz ES-ERED.
➢ Wszystkie ES-ERED można testować odpowiednio w powyższym systemie reakcji lub przy użyciu zestawu ERED Screening Kit (SynKit ERED).
➢ Wszystkie rodzaje ES-ERED odpowiadające różnym optymalnym warunkom reakcji powinny być badane indywidualnie.
➢ Wysokie stężenie substratu lub produktu może hamować aktywność ES-ERED. Hamowanie to można jednak złagodzić poprzez partiowe dodawanie substratu.
Przykład 1 (α,β-nienasycone aldehydy lub ketony)(1):
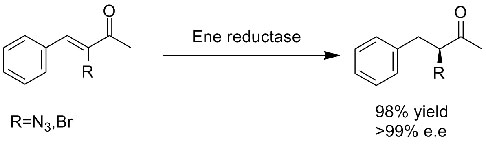
Przykład 2 (α,β-nienasycone kwasy karboksylowe i ich pochodne)(2):
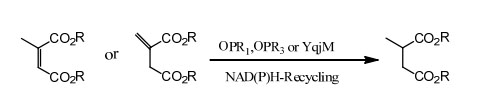
Przechowywać przez 2 lata w temperaturze poniżej -20℃.
Nigdy nie narażaj się na kontakt z ekstremalnymi warunkami, takimi jak: wysoka temperatura, wysokie/niskie pH i wysokie stężenie rozpuszczalników organicznych.
1. Lucidio C, Fardelone J, Augusto R i in. J.Mol.Catal.B:Enzym., 2004, 29:41-45.
2. Stueckler C, Hall M, Ehammer H, i in. .Org.Lett, 2007, 9(26): 5409-5411.